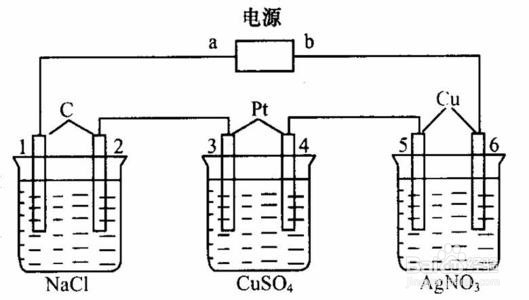
1、判断正负极,阴阳极,负极失去电子,电解池正相反,阳极失去电子,电流的流向与电子的流向相反。
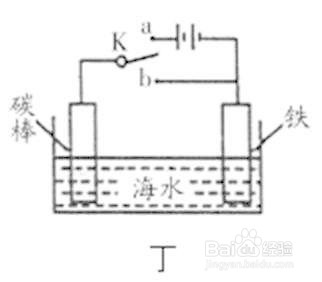
2、判断溶液内部离子的走向,除了得失电子判断,还可以用“电子与阴离子沿电极环绕成圈”的结论去判断。
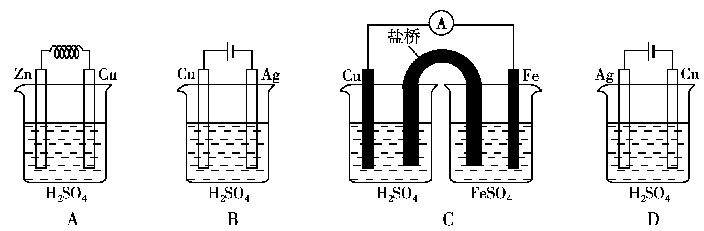
3、由以上信息,加上题目所提示的生成物,反应物,结合氧化还原反应的知识,我们便能够大致写出正负(阴阳)极反应式和总反应式。
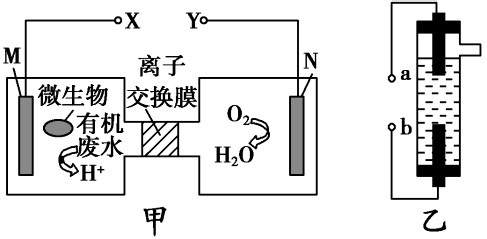
4、电解池反应需要记住两个放\生电顺序,由大到小发生反应,H离子和水的反应需要记一下,以便于书写电解反应式。
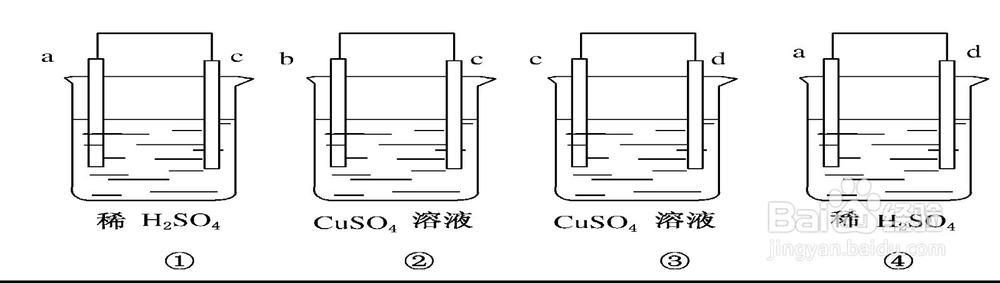
5、金属活性电极作原电池在酸性条件下发生析氢腐蚀,在碱性(中性)条件发生吸氧腐蚀,不会与溶质反应。

6、遇到多个电池或电解池在一块,有外接电源则全是电解池,无外接电源则有一个会是原电池,剩下全是电解池。